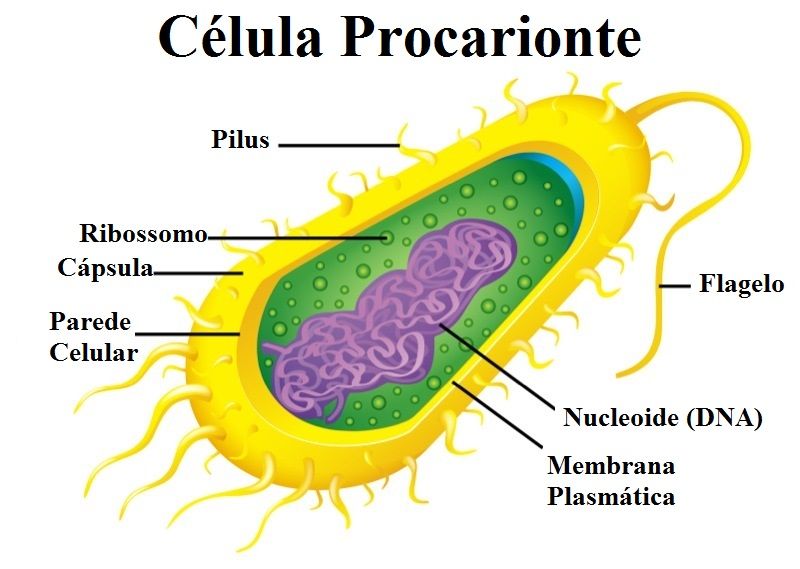
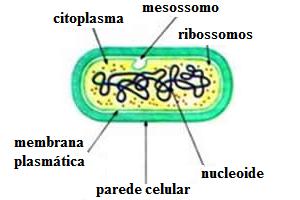
Átomos: Número atômico, número de massa, isótopos, massa atômica
No final da postagem tem uma videoaula bem interessante, vale a pena conferir.
Dica: Estou atualizando o Conteúdo Programático completo do ENEM e além disso, para você que não esta encontrando todo o conteúdo do Enem ou prefere estudar por apostilas dá uma olhada nesta apostilas para ENEM do site Apostilas Opção é bem interessante.
Bons estudos!
Átomos: Número atômico, número de massa, isótopos, massa atômica
Número Atômico e Número de Massa
Os modelos atômicos propostos indicam que os átomos diferem entre si pelo número de prótons, nêutrons e elétrons que contêm. Para identificar o número dessas partículas, são determinados o número de massa e o número atômico.
As massas atômicas são determinadas por comparação das massas dos átomos com um padrão de massas que equivale a 1/12 da massa do átomo de carbono. O valor numérico da massa atômica é muito próximo do valor do número de massa.
 O número de massa e o número atômico
O número de massa e o número atômico
Um átomo pode ser definido mediante dois números:
O número atômico, cujo símbolo é Z, é o número de prótons que tem um átomo. Como o átomo isolado é neutro, o número de prótons coincide com o número de elétrons.
Z = número de prótons = número de elétrons (para um átomo neutro)
O número de massa, cujo símbolo é A, é o número de partículas que tem um átomo em seu núcleo. É a soma de prótons e nêutrons.
A = número de massa = número de prótons + número de nêutrons
A = Z + N
O que realmente identifica o elemento a que pertence o átomo é o número atômico (Z). O valor de A é útil, mas não identifica de que elemento é o átomo em questão.
Representação abreviada dos átomos





.jpg) Estado Gasoso: a movimentação das moléculas nesse estado é bem maior que no estado líquido ou sólido. Se variarmos a pressão exercida sobre um gás podemos aumentar ou diminuir o volume dele, sendo assim, pode-se dizer que sofre compressão e expansão facilmente. Os elementos gasosos tomam a forma do recipiente que os contém.
Estado Gasoso: a movimentação das moléculas nesse estado é bem maior que no estado líquido ou sólido. Se variarmos a pressão exercida sobre um gás podemos aumentar ou diminuir o volume dele, sendo assim, pode-se dizer que sofre compressão e expansão facilmente. Os elementos gasosos tomam a forma do recipiente que os contém.
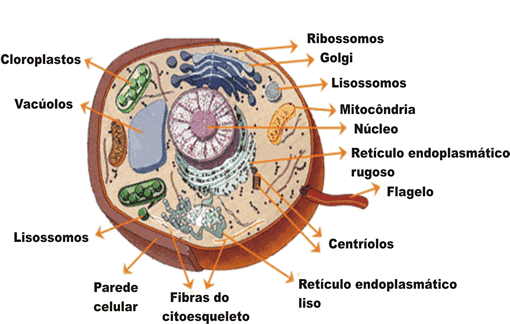 Já as células eucarióticas, possuem maior tamanho e complexidade, a começar pelo núcleo individualizado, envolvido pela carioteca. Seu citoplasma é interconectado por uma rede de tubos e canais membranosos e é onde, além de ribossomos, também são encontradas mitocôndrias, retículo endoplasmático granuloso e não granuloso, complexo golgiense, lisossomos, peroxissomos, centríolos, dentre outras organelas.
Já as células eucarióticas, possuem maior tamanho e complexidade, a começar pelo núcleo individualizado, envolvido pela carioteca. Seu citoplasma é interconectado por uma rede de tubos e canais membranosos e é onde, além de ribossomos, também são encontradas mitocôndrias, retículo endoplasmático granuloso e não granuloso, complexo golgiense, lisossomos, peroxissomos, centríolos, dentre outras organelas.